ЩњаХШыУХ(Жў)ЁЊЁЊЪЙгУlimmaЁЂGlimmaКЭedgeR,RNA-seqЪ§ОнЗжЮі
ЮФеТФПТМ
вЛЁЂМђНщ
МђЕЅЧвИпаЇЕиЗжЮіRNA ВтађЪ§ОнЕФФмСІЪЧЩњаХЕФКЫаФгХЪЦжЎвЛЁЃЭЈГЃдкЛёЕУRNA-seqЛљвђБэДяОиеѓКѓ,ЭЈГЃашвЊЖдЪ§ОнНјааЪ§ОндЄДІРэЁЂЬНЫїадЪ§ОнЗжЮіЁЂВювьБэДяМьбщвдМАЭЈТЗЗжЮі,вдЕУЕНПЩвдАяжњНјвЛВНЪдбщКЭбщжЄбаОПЕФНсЙћЁЃЮДРДМИЦЊНЋНщЩмЪЙгУedgeRАќ,limmaАќ,GlimmaАќЖдRNA-seqЪ§ОнеЙПЊЗжЮі,ДгдЪММЦЪ§(counts)жаЭкОђЩњЮябЇвтвх
ЖўЁЂЪ§ОнБГОА
дкБОЦЊЮФеТжа,УшЪіСЫвЛИігУгкЗжЮіRNA-seqЪ§ОнЕФedgeR - limmaЙЄзїСїГЬ,ЪЙгУЛљвђЫЎЦНЕФМЦЪ§(gene-level counts)зїЮЊЪфШы,ОЙ§дЄДІРэКЭЬНЫїадЪ§ОнЗжЮі,ШЛКѓЕУЕНВювьБэДя(DE)ЛљвђКЭЛљвђБэДяЬиеї(gene signatures)ЕФСаБэЁЃGlimmaАќ(Su et al. 2017)ЬсЙЉЕФНЛЛЅЪНЭМБэПЩвдЭЌЪБГЪЯжећЬхбљБОВуУцгыЕЅИіЛљвђВуУцЕФЪ§Он,ЯрЖдОВЬЌЕФRЭМБэЖјбд,ИќБугкЮвУЧЬНЫїИќЖрЕФЯИНкЁЃ
ДЫЙЄзїСїГЬжаЮвУЧЗжЮіЕФЪ§ОнРДздSheridanЕШШЫЕФЪЕбщ(2015)(Sheridan et al. 2015),ЫќАќКЌШ§ИіЯИАћШК,МДЛљЕз(basal)ЁЂЙмЧЛзцЯИАћ(liminal progenitor, LP)КЭГЩЪьЙмЧЛ(mature luminal, ML)ЁЃЯИАћШКНдЗжбЁздДЦадДІХЎаЁЪѓЕФШщЯй,УПжжЖМЩшШ§ИіЩњЮябЇжиИДЁЃRNAбљЦЗЗжШ§ИіХњДЮЪЙгУIllumina HiSeq 2000НјааВтађ,ЕУЕНГЄЮЊ100МюЛљЖдЕФЕЅЖЫађСаЦЌЖЮЁЃ
Ш§ЁЂГѕЪМХфжУ
library(limma)
library(Glimma)
library(edgeR)
library(Mus.musculus)
ЫФЁЂЪ§ОнећКЯ
1ЁЂЪ§ОнЯТди
Ъ§ОнРДдД:https://www.ncbi.nlm.nih.gov/geo/download/?acc=GSE63310&format=file ЯТдиGSE63310_RAW.tarЗХдквЛЖЈЕФЮФМўМа
2ЁЂНтбЙЮФМў
setwd("D:\\RData\\prac002")#ЩшжУЕБЧАТЗОЖ,ЯТдиЪ§ОндкИУЮФМўМаЯТ
utils::untar("GSE63310_RAW.tar", exdir = ".")
files<-c("GSM1545535_10_6_5_11.txt", "GSM1545536_9_6_5_11.txt", "GSM1545538_purep53.txt",
"GSM1545539_JMS8-2.txt", "GSM1545540_JMS8-3.txt", "GSM1545541_JMS8-4.txt",
"GSM1545542_JMS8-5.txt", "GSM1545544_JMS9-P7c.txt", "GSM1545545_JMS9-P8c.txt")
for(i in paste(files,".gz",sep=""))
R.utils::gunzip(i,overwrite=TURE)
УПвЛИіЮФБОЮФМўОљЮЊЖдгІбљЦЗЕФдЪМЛљвђЫЎЦНМЦЪ§ОиеѓЁЃашвЊзЂвтЮвУЧЕФетДЮЗжЮіНіАќКЌСЫДЫЪЕбщжаЕФbasalЁЂLPКЭMLбљЦЗ(ПЩМћЯТЗНЫљЪОЮФМўУћ)ЁЃ
files<-c("GSM1545535_10_6_5_11.txt", "GSM1545536_9_6_5_11.txt",
"GSM1545538_purep53.txt", "GSM1545539_JMS8-2.txt",
"GSM1545540_JMS8-3.txt", "GSM1545541_JMS8-4.txt",
"GSM1545542_JMS8-5.txt", "GSM1545544_JMS9-P7c.txt",
"GSM1545545_JMS9-P8c.txt")
read.delim(files[1],nrow=5)#ВщПДЕМШыЪ§Он
дЫааНсЙћ
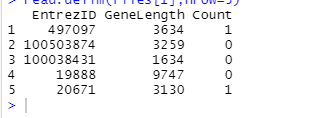
ЯрБШгкЗжБ№ЖСШыетОХИіЮФБОЮФМўШЛКѓКЯВЂЮЊвЛИіМЦЪ§Оиеѓ,edgeRЬсЙЉСЫИќЗНБуЕФЭООЖ,ЪЙгУreadDGEКЏЪ§МДПЩвЛВНЭъГЩЁЃЕУЕНЕФDGEListЖдЯѓжаАќКЌвЛИіМЦЪ§Оиеѓ,ЫќЕФ27179ааЗжБ№ЖдгІУПИіЛљвђВЛжиИДЕФEntrezЛљвђID,ОХСаЗжБ№ЖдгІДЫЪЕбщжаЕФУПИібљЦЗЁЃ
class(x)
dim(x)
дЫааНсЙћ
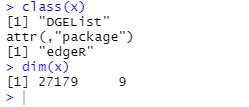
зЂ:ШчЙћЪ§ОнВЛЪЧУПИібљБОвЛИіЮФМўЕФаЮЪН,ЖјЪЧАќКЌЫљгабљБОЕФММЪѕЕФЮФМў,дђПЩвдЯШНЋЮФМўЖСШыR,дйЪЙгУDGEListКЏЪ§зЊЛЛЮЊвЛИіDGEListЖдЯѓ
3ЁЂзщжЏбљБОаХЯЂ
ЮЊНјааЯТгЮЗжЮі,ашвЊНЋгаЙиЪЕбщЩшМЦЕФбљЦЗаХЯЂгыМЦЪ§ОиеѓЕФСаЙиСЊЦ№РДЁЃетРяашвЊАќРЈИїжжЖдБэДяЫЎЦНгагАЯьЕФЪЕбщБфСП,ЮоТлЪЧЩњЮяБфСПЛЙЪЧММЪѕБфСПЁЃР§Шч,ЯИАћРраЭ(дкетИіЪЕбщжаЪЧbasalЁЂLPКЭML)ЁЂЛљвђаЭ(вАЩњаЭЁЂЧУГ§)ЁЂБэаЭ(МВВЁзДЬЌЁЂадБ№ЁЂФъСф)ЁЂбљЦЗДІРэ(гУвЉЁЂЖдее)КЭХњДЮаХЯЂ(ШчЙћбљЦЗЪЧдкВЛЭЌЪБМфЕуНјааЪеМЏКЭЗжЮіЕФ,ашвЊМЧТМНјааЪЕбщЕФЪБМф)ЕШЁЃ
ЮвУЧЕФDGEListЖдЯѓжаАќКЌЕФsamplesЪ§ОнПђЭЌЪБДцДЂСЫЯИАћРраЭ(group)КЭХњДЮ(ВтађгОЕРlane)аХЯЂ,УПжжаХЯЂЖМАќКЌШ§ИіВЛЭЌЕФЫЎЦНЁЃдкx$samplesжа,ГЬађЛсздЖЏМЦЫуУПИібљЦЗЕФЮФПтДѓаЁ(МДбљЦЗЕФзмађСаМЦЪ§),ЙщвЛЛЏЯЕЪ§ЛсБЛдЄЯШЩшжУЮЊ1ЁЃ ЮЊСЫЗНБудФЖС,ЮвУЧДгDGEListЖдЯѓxЕФСаУћжаЩОШЅСЫGEOбљЦЗID(GSM*)ЁЃ
samplenames<-substring(colnames(x),12,nchar(colnames(x)))
colnames(x)<-samplenames
group<-as.factor(c("LP", "ML", "Basal", "Basal", "ML", "LP",
"Basal", "ML", "LP"))
x$samples$group<-group
lane<-as.factor(rep(c("L004","L006","L008"),c(3,4,2)))
x$samples$lane<-lane
x$samples
дЫааНсЙћ
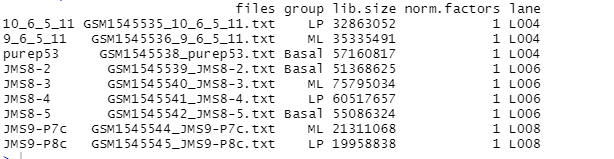
4.зщжЏЛљвђзЂЪЭ
DGEListЖдЯѓжаЕФЕкЖўИіЪ§ОнПђУћЮЊgenes,гУгкДцДЂгыМЦЪ§ОиеѓЕФааЯрЙиСЊЕФЛљвђаХЯЂЁЃ ЮЊМьЫїетаЉаХЯЂ,ЮвУЧПЩвдЪЙгУЬиЖЈЮяжжЕФзЂЪЭАќ,БШШчаЁЪѓЕФMus.musculus (Bioconductor Core Team 2016b)(ЛђШЫРрЕФHomo.sapiens (Bioconductor Core Team 2016a));ЛђепвВПЩвдЪЙгУbiomaRt Аќ (Durinck et al. 2005, 2009),ЫќЭЈЙ§НгШыEnsembl genomeЪ§ОнПтРДНјааЛљвђзЂЪЭЁЃ
ПЩвдМьЫїЕФаХЯЂРраЭАќРЈЛљвђЗћКХ(gene symbols)ЁЂЛљвђУћГЦ(gene names)ЁЂШОЩЋЬхУћГЦКЭЮЛжУЁЂEntrezЛљвђIDЁЂRefseqЛљвђIDКЭEnsemblЛљвђIDЕШЁЃbiomaRtжївЊЭЈЙ§EnsemblЛљвђIDНјааМьЫї,ЖјMus.musculusАќКЌРДздВЛЭЌРДдДЕФаХЯЂ,дЪаэгУЛЇДгВЛЭЌЛљвђIDжабЁдёФГвЛжжзїЮЊМьЫїМќЁЃ
гыШЮКЮЛљвђIDвЛбљ,EntrezЛљвђIDПЩФмВЛФмвЛЖдвЛЕиЦЅХфЮвУЧЯыЛёЕУЕФЛљвђаХЯЂЁЃдкДІРэжЎЧА,МьВщжиИДЕФЛљвђIDКЭХЊЧхГўжиИДЕФРДдДЗЧГЃживЊЁЃЮвУЧЕФЛљвђзЂЪЭжаАќКЌ28ИіФмЦЅХфЕНЖрИіВЛЭЌШОЩЋЬхЕФЛљвђ(БШШчЛљвђGm1987ЙиСЊгкШОЩЋЬхchr4КЭchr4_JH584294_random,аЁRNA Mir5098ЙиСЊгкchr2,chr5,chr8,chr11КЭchr17)ЁЃ ЮЊСЫДІРэжиИДЕФЛљвђID,ЮвУЧПЩвдКЯВЂРДздЖржиЦЅХфЛљвђЕФЫљгаШОЩЋЬхаХЯЂ,БШШчНЋЛљвђGm1987ЗжХфЕНchr4 and chr4_JH584294_random,ЛђбЁШЁЦфжавЛЬѕШОЩЋЬхРДДњБэОпгажиИДзЂЪЭЕФЛљвђЁЃЮЊСЫМђЕЅЦ№Мћ,ЮвУЧбЁдёКѓеп,БЃСєУПИіЛљвђIDЕквЛДЮГіЯжЕФаХЯЂЁЃ
дкДЫР§згжа,зЂЪЭгыЪ§ОнЖдЯѓжаЕФЛљвђЫГађЪЧЯрЭЌЕФЁЃШчЙћгЩгкШБЪЇКЭ/ЛђжиаТХХСаЛљвђIDЕМжТЦфЫГађВЛвЛжТ,ЮвУЧПЩвдгУmatchКЏЪ§РДе§ШЗХХађЛљвђЁЃШЛКѓ,ЮвУЧНЋЛљвђзЂЪЭЕФЪ§ОнПђЬэМгЕНDGEListЖдЯѓ,Ъ§ОнЕФећКЯОЭЭъГЩСЫ,ДЫЪБЕФЪ§ОнЖдЯѓжаКЌгадЪММЦЪ§Ъ§ОнвдМАЯрЙиЕФбљЦЗаХЯЂКЭЛљвђзЂЪЭЁЃ
geneid<-rownames(x)
genes<-select(Mus.musculus,keys=geneid,columns=
c("SYMBOL","TXCHROM"),
keytype = "ENTREZID")
head(genes)
genes<-genes[!duplicated(genes$ENTREZID),]
x$genes<-genes
x
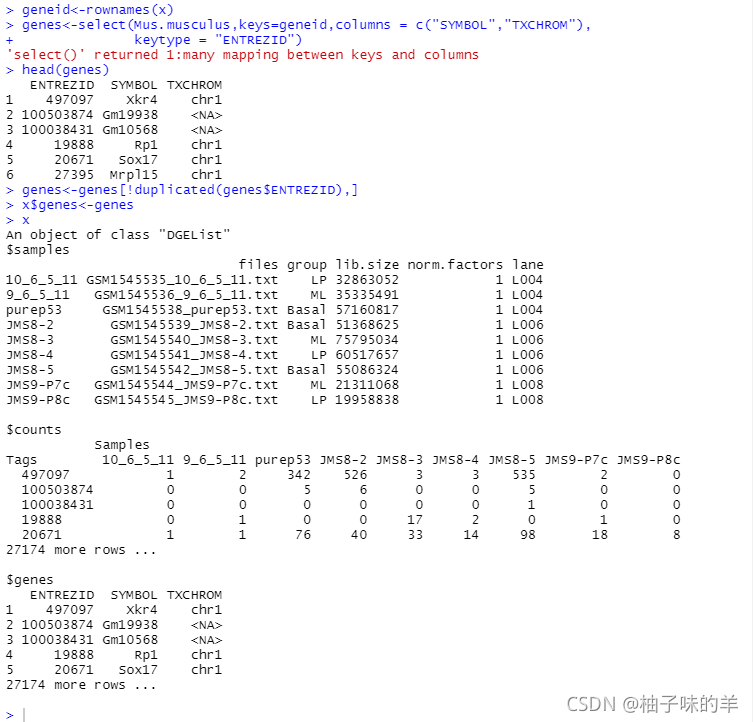
ЮхЁЂЪ§ОндЄДІРэ
1ЁЂдЪМЪ§ОнГпЖШзЊЛЛ
гЩгкИќЩюЕФВтађзмЛсВњЩњИќЖрЕФађСаЦЌЖЮ,дкВювьБэДяМАЯрЙиЕФЗжЮіжа,ЮвУЧКмЩйжБНгЪЙгУађСаЪ§ЁЃдкЪЕМЪВйзїЪБ,ЮвУЧЭЈГЃНЋдЪМЕФађСаЪ§НјааЙщвЛЛЏ,РДЯћГ§ВтађЩюЖШЫљЕМжТЕФВювьЁЃЭЈГЃБЛЪЙгУЕФЗНЗЈгаЛљгкађСаЕФCPM(counts per million)ЁЂlog-CPMЁЂFPKM(fragments per kilobase of transcript per million),КЭЛљгкзЊТМБОЪ§ФПЕФRPKM(reads per kilobase of transcript per million)ЁЃ
ЮвУЧдкЗжЮіжаЭЈГЃЪЙгУCPMКЭlog-CPMзЊЛЛЁЃЫфШЛRPKMКЭFPKMПЩвдаЃе§ЛљвђГЄЖШЧјБ№ЕФгАЯь,ЕЋCPMКЭlog-CPMжЛЪЙгУМЦЪ§ОиеѓМДПЩМЦЫу,ЧввбзувдТњзуЮвУЧЫљЙизЂЕФБШНЯЕФашвЊЁЃМйЩшВЛЭЌЬѕМўжЎМфМєНгвьЙЙЬх(isoform)ЕФБэДяБШР§УЛгаБфЛЏ,ВювьБэДяЗжЮіЙизЂЕФЪЧЭЌвЛЛљвђдкВЛЭЌЬѕМўжЎМфБэДяЫЎЦНЕФЯрЖдВювь,ЖјВЛЪЧБШНЯЖрИіЛљвђжЎМфЕФВювьЛђВтЖЈОјЖдБэДяСПЁЃЛЛЖјбджЎ,ЛљвђГЄЖШдкЮвУЧНјааБШНЯЕФВЛЭЌзщжЎМфЪЧЪМжеВЛБфЕФ,ЧвШЮКЮЙлВтЕНЕФВювьЖМРДздгкВЛЭЌзщЕФЬѕМўЕФБфЛЏЖјВЛЪЧЛљвђГЄЖШЕФБфЛЏЁЃ
ЮвУЧЪЙгУedgeRжаЕФcpmКЏЪ§НЋдЪММЦЪ§зЊЛЛЮЊCPMКЭlog-CPMжЕЁЃШчЙћПЩвдЬсЙЉЛљвђГЄЖШаХЯЂ,RPKMжЕЕФМЦЫувВКЭCPMжЕЕФМЦЫувЛбљМђЕЅ,жЛашЪЙгУedgeRжаЕФrpkmКЏЪ§ЁЃ
cpm<-cpm(x)
lcpm<-cpm(x,log=TRUE,prior.count = 2)
ЖдгквЛИіЛљвђ,CPMжЕЮЊ1ЯрЕБгкдкБОЪЕбщВтађЩюЖШзюЕЭЕФбљЦЗжа(JMS9-P8c, ЮФПтДѓаЁдМ2ЧЇЭђ)га20ИіМЦЪ§,ЛђепдкВтађЩюЖШзюИпЕФбљЦЗжа(JMS8-3,ЮФПтДѓаЁдМ7.6ЧЇЭђ)га76ИіМЦЪ§ЁЃ
ЕБЩшжУlog=TRUEЪБ,cpmКЏЪ§ЛсИјCPMжЕМгЩЯвЛИіУжВЙжЕВЂНјааlog2зЊЛЛЁЃФЌШЯЕФУжВЙжЕЪЧ2/L,Цфжа2ЪЧЁАдЄЯШМЦЪ§ЁБ,ЖјLЪЧбљБОЮФПтДѓаЁ(вдАйЭђМЦ)ЕФЦНОљжЕ,Ыљвдlog-CPMжЕЪЧИљОнCPMжЕЭЈЙ§log2(CPM + 2/L)МЦЫуЕУЕНЕФЁЃетбљЕФМЦЫуЗНЪНПЩвдШЗБЃШЮвтСНИіОпгаЯрЭЌCPMжЕЕФађСаЦЌЖЮМЦЪ§ЕФlog-CPMжЕвВЯрЭЌЁЃУжВЙжЕЕФЪЙгУПЩвдБмУтЖдСуШЁЖдЪ§,ВЂФмЪЙЫљгабљБОМфЕФЖдЪ§БЖЪ§БфЛЏ(log-fold-change)Яђ0ЭЦвЦЖјМѕаЁЕЭБэДяЛљвђМфЮЂаЁМЦЪ§БфЛЏДјРДЕФОоДѓЕФЮБВювьад,етЖдгкЛцжЦЬНЫїадЭМБэКмгаАяжњЁЃдкетИіЪ§ОнМЏжа,ЦНОљЕФбљБОЮФПтДѓаЁЪЧ4.55ЧЇЭђ,ЫљвдLдМЕШгк45.5,ЧвУПИібљБОжаЕФзюаЁlog-CPMжЕЮЊlog2(2/45.5) = -4.51ЁЃЛЛЖјбджЎ,дкМгЩЯСЫдЄЯШМЦЪ§УжВЙжЕКѓ,ДЫЪ§ОнМЏжаЕФСуБэДяМЦЪ§ЖдгІЕФlog-CPMжЕЮЊ-4.51:
L<-mean(x$samples$lib.size)* 1e-6
M<-median(x$samples$lib.size)*1e-6
c(L,M)
summary(lcpm)
НсЙћеЙЪО

дкНгЯТРДЕФЯпадФЃаЭЗжЮіжа,ЪЙгУlimmaЕФvoomКЏЪ§ЪБвВЛсгУЕНlog-CPMжЕ,ЕЋvoomЛсФЌШЯЪЙгУИќаЁЕФдЄЯШМЦЪ§жиаТМЦЫуздМКЕФlog-CPMжЕЁЃ
2ЁЂЩОГ§ЕЭБэДяЛљвђ
ЫљгаЪ§ОнМЏжаЖМЛьгаБэДяЕФЛљвђгыВЛБэДяЕФЛљвђЁЃЮвУЧЯывЊМьВтдквЛжжЬѕМўжаБэДяЕЋдкСэвЛжжЬѕМўжаВЛБэДяЕФЛљвђ,ЕЋвВгавЛаЉЛљвђдкЫљгабљЦЗжаЖМВЛБэДяЁЃЪЕМЪЩЯ,етИіЪ§ОнМЏжа19%ЕФЛљвђдкЫљгаОХИібљЦЗжаЕФМЦЪ§ЖМЪЧСуЁЃ
table(rowSums(x$counts==0)==9)
log-CPMжЕЕФЗжВМЭМБэЯдЪОУПИібљБОжаКмДѓвЛВПЗжЛљвђЖМЪЧВЛБэДяЛђепБэДяГЬЖШЯрЕБЕЭЕФ,ЫќУЧЕФlog-CPMжЕЗЧГЃаЁЩѕжСЪЧИКЕФ
дкШЮКЮбљБОжаЖМУЛгазуЙЛЖрЕФађСаЦЌЖЮЕФЛљвђгІИУДгЯТгЮЗжЮіжаЙ§ТЫЕєЁЃетбљзіЕФдвђгаКУМИИіЁЃ ДгЩњЮябЇЕФНЧЖШРДПД,дкШЮКЮЬѕМўЯТЕФБэДяЫЎЦНЖМВЛОпгаЩњЮябЇвтвхЕФЛљвђЖМВЛжЕЕУЙизЂ,вђДЫзюКУКіТдЁЃ ДгЭГМЦбЇЕФНЧЖШРДПД,ШЅГ§ЕЭБэДяМЦЪ§ЛљвђЪЙЪ§ОнжаЕФОљжЕ - ЗНВюЙиЯЕПЩвдЕУЕНИќОЋШЗЕФЙРМЦ,ВЂЧвЛЙМѕЩйСЫЯТгЮЕФВювьБэДяЗжЮіжаашвЊНјааЕФЭГМЦМьбщЕФЪ§СПЁЃ
edgeRАќжаЕФfilterByExprКЏЪ§ЬсЙЉСЫздЖЏЙ§ТЫЛљвђЕФЗНЗЈ,ПЩБЃСєОЁПЩФмЖрЕФгазуЙЛБэДяМЦЪ§ЕФЛљвђЁЃ
keep.exprs<-filterByExpr(x,group = group)
x<-x[keep.exprs,,keep.lib.sizes=FALSE]
dim(x)
ДЫКЏЪ§ФЌШЯбЁШЁзюаЁЕФзщФкЕФбљБОЪ§СПЮЊзюаЁбљБОЪ§,БЃСєжСЩйдкетИіЪ§СПЕФбљБОжага10ИіЛђИќЖрМЦЪ§ЕФЛљвђЁЃЪЕМЪНјааЙ§ТЫЪБ,ЪЙгУЕФЪЧCPMжЕЖјВЛЪЧБэДяМЦЪ§,вдБмУтЖдзмађСаЪ§ДѓЕФбљБОЕФЦЋЯђадЁЃдкетИіЪ§ОнМЏжа,змађСаЪ§ЕФжаЮЛЪ§ЪЧ5.1ЧЇЭђ,Чв10/51дМЕШгк0.2,ЫљвдfilterByExprКЏЪ§БЃСєдкжСЩйШ§ИібљБОжаCPMжЕДѓгкЕШгк0.2ЕФЛљвђЁЃдкЮвУЧЕФДЫДЮЪЕбщжа,вЛИіОпгаЩњЮябЇвтвхЕФЛљвђашвЊдкжСЩйШ§ИібљБОжаБэДя,вђЮЊШ§жжЯИАћРраЭзщФкИїгаШ§ИіжиИДЁЃЙ§ТЫЕФуажЕШЁОігкВтађЩюЖШКЭЪЕбщЩшМЦЁЃШчЙћбљБОзмБэДяМЦЪ§СПдіДѓ,ФЧУДПЩвдбЁдёИќЕЭЕФCPMуажЕ,вђЮЊИќДѓЕФзмБэДяМЦЪ§СПЬсЙЉСЫИќКУЕФЗжБцТЪРДЬНОПИќЖрБэДяЫЎЦНИќЕЭЕФЛљвђЁЃ
ЪЙгУетИіБъзМ,ЛљвђЕФЪ§СПМѕЩйЕНСЫ16624Иі,дМЮЊПЊЪМЪБЪ§СПЕФ60%ЁЃЙ§ТЫКѓЕФlog-CPMжЕЯдЪОГіУПИібљБОЕФЗжВМЛљБОЯрЭЌ(ЯТЭМBВПЗж)ЁЃашвЊзЂвтЕФЪЧ,ДгећИіDGEListЖдЯѓжаШЁзгМЏЪБЭЌЪБЩОГ§СЫБЛЙ§ТЫЕФЛљвђЕФМЦЪ§КЭЦфЯрЙиЕФЛљвђаХЯЂЁЃСєЯТЕФЛљвђЯрЖдгІЕФЛљвђаХЯЂКЭМЦЪ§дкЙ§ТЫКѓЕФDGEListЖдЯѓжаБЛБЃСєЁЃ
ЛцЭМДњТы
lcpm.cutoff<-log2(10/M+2/L)
library(RColorBrewer)
nsamples<-ncol(x)
col<-brewer.pal(nsamples,"Paired")
par(mfrow=c(1,2))
plot(density(lcpm[,1]),col=col[1],lwd=2,ylim=c(0,0.26),las=2,main="",xlab="")
title(main = "A.Raw data",xlab="Log-cpm")
abline(v=lcpm.cutoff,lty=3)
for (i in 2:nsamples){
den<-density(lcpm[,i])
lines(den$x,den$y,col=col[i],lwd=2)
}
legend("topright",samplenames,text.col = col,bty = "n")
lcpm<-cpm(x,log=TRUE)
plot(density(lcpm[,1]),col=col[1],lwd=2,ylim=c(0,0.26),las=2,main="",xlab="")
title(main = "B.Filtered data",xlab="Log-cpm")
abline(v=lcpm.cutoff,lty=3)
for (i in 2:nsamples) {
den<-density(lcpm[,i])
lines(den$x,den$y,col=col[i],lwd=2)
}
legend("topright",samplenames,text.col = col,bty="n")
дЫааНсЙћ
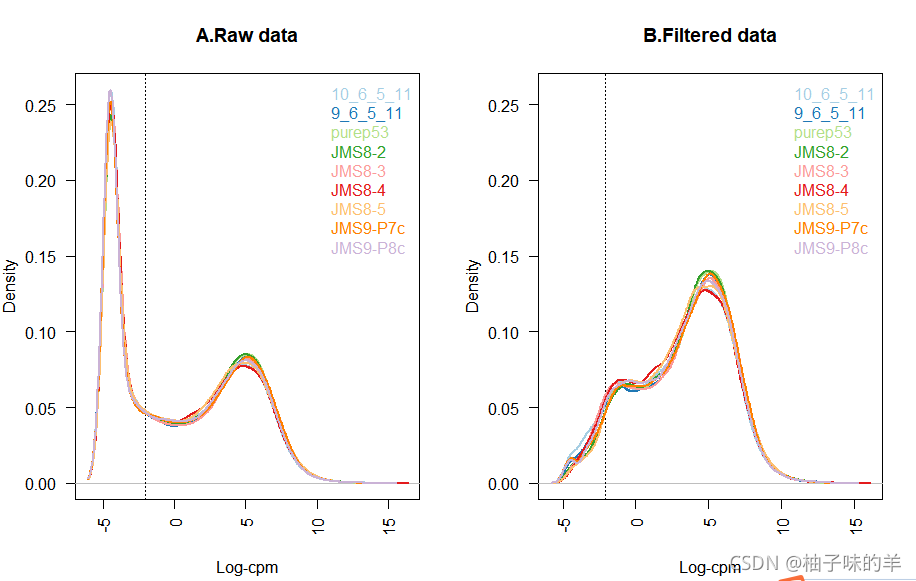
УПИібљБОЙ§ТЫЧАЕФдЪМЪ§Он(A)КЭЙ§ТЫКѓ(B)ЕФЪ§ОнЕФlog-CPMжЕУмЖШЁЃЪњжБащЯпБъГіСЫЙ§ТЫВНжшжаЫљгУуажЕ(ЯрЕБгкCPMжЕЮЊдМ0.2)ЁЃ
3ЁЂЙщвЛЛЏЛљвђБэДяЗжВМ
дкбљЦЗжЦБИЛђВтађЙ§ГЬжа,ВЛОпБИЩњЮябЇвтвхЕФЭтВПвђЫиЛсгАЯьЕЅИібљЦЗЕФБэДяЁЃБШШчЫЕ,дкЪЕбщжаЕквЛХњжЦБИЕФбљЦЗЛсзмЬхЩЯБэДяИпгкЕкЖўХњжЦБИЕФбљЦЗЁЃВювьБэДяЗжЮіМйЩшЫљгабљЦЗБэДяжЕЕФЗЖЮЇКЭЗжВМЖМгІЕБЯрЫЦЁЃЮвУЧашвЊНјааЙщвЛЛЏРДШЗБЃећИіЪЕбщжаУПИібљБОЕФБэДяЗжВМЖМЯрЫЦЁЃ
УмЖШЭМКЭЯфЯпЭМЕШеЙЪОУПИібљЦЗЛљвђБэДяСПЗжВМЕФЭМБэПЩвдгУгкХаЖЯЪЧЗёгабљЦЗКЭЦфЫћбљЦЗЗжВМгаВювьЁЃдкДЫЪ§ОнМЏжа,ЫљгабљЦЗЕФlog-CPMЗжВМЖМКмЯрЫЦЁЃ
ОЁЙмШчДЫ,ЮвУЧвРШЛашвЊЪЙгУedgeRжаЕФcalcNormFactorsКЏЪ§,гУTMM(Robinson and Oshlack 2010)ЗНЗЈНјааЙщвЛЛЏЁЃДЫДІМЦЫуЕУЕНЕФЙщвЛЛЏЯЕЪ§БЛгУзїЮФПтДѓаЁЕФЫѕЗХЯЕЪ§ЁЃЕБЮвУЧЪЙгУDGEListЖдЯѓЪБ,етаЉЙщвЛЛЏЯЕЪ§БЛздЖЏДцДЂдкx s a m p l e s samples samplesnorm.factorsЁЃЖдДЫЪ§ОнМЏЖјбд,TMMЙщвЛЛЏЕФзїгУБШНЯЮТКЭ,етЬхЯждкЫљгаЕФЫѕЗХвђзгЖМЯрЖдНгНќ1ЁЃ
x<-calcNormFactors(x,method="TMM")#TMMЙщвЛЛЏДІРэ
x$sample$norm.factors
#ЮЊСЫИќКУЕиеЙЪОГіЙщвЛЛЏЕФаЇЙћ,ЮвУЧИДжЦСЫЪ§ОнВЂНјааСЫШЫЙЄЕїећ,
#ЪЙЕУЕквЛИібљЦЗЕФМЦЪ§МѕЩйЕНСЫЦфдЪМжЕЕФ5%,ЖјЕкЖўИібљЦЗдіДѓЕНСЫ5БЖЁЃ
#вЊзЂвтдкЪЕМЪЕФЪ§ОнЗжЮіСїГЬжа,ВЛгІЕБНјааетбљЕФВйзїЁЃ
x2 <- x
x2$samples$norm.factors <- 1
x2$counts[,1] <- ceiling(x2$counts[,1]*0.05)
x2$counts[,2] <- x2$counts[,2]*5
#ЯТЭМЯдЪОСЫУЛгаОЙ§ЙщвЛЛЏЕФгыОЙ§СЫЙщвЛЛЏЕФЪ§ОнЕФБэДяЗжВМ
#ЦфжаЙщвЛЛЏЧАВЛЭЌбљБОЕФЗжВМУїЯдВЛЭЌ,ЖјЙщвЛЛЏКѓБШНЯЯрЫЦЁЃ
#ДЫДІ,ОЙ§ЮвУЧШЫЙЄЕїећЕФЕквЛИібљЦЗЕФTMMЫѕЗХЯЕЪ§0.06ЗЧГЃаЁ
#ЖјЕкЖўИібљЦЗЕФЫѕЗХЯЕЪ§6.08КмДѓ,ЫќУЧЖМВЂВЛНгНќ1ЁЃ
par(mfrow=c(1,2))
lcpm<-cpm(x2,log=TRUE)
boxplot(lcpm,las=2,col=col,main="")
title(main="A.Example:Unnormalised data",ylab="Log-cpm")
x2<-calcNormFactors(x2)
x2$samples$norm.factors
lcpm<-cpm(x2,log=TRUE)
boxplot(lcpm,las=2,col=col,main="")
title(main="B.Example:Normalised data",ylab="Log-cpm")
дЫааНсЙћ
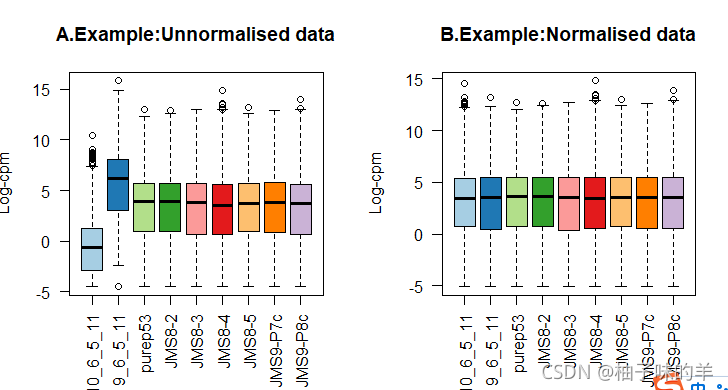
бљР§Ъ§Он:log-CPMжЕЕФЯфЯпЭМеЙЪОСЫЮДОЙщвЛЛЏЕФЪ§Он(A)МАЙщвЛЛЏКѓЕФЪ§Он(B)жаУПИібљБОЕФБэДяЗжВМЁЃЪ§ОнМЏОЙ§Еїећ,бљБО1КЭ2жаЕФБэДяМЦЪ§ЗжБ№БЛЫѕЗХЕНЦфдЪМжЕЕФ5%КЭ500%ЁЃ
4ЁЂЖдбљБОЕФЮоМрЖНОлРр
дкЮвУЧПДРД,гУгкМьВщЛљвђБэДяЗжЮіЕФзюживЊЕФЬНЫїадЭМБэжЎвЛБуЪЧMDSЭМ,ЛђРрЫЦЕФЭМЁЃетжжЭМБэЪЙгУЮоМрЖНОлРрЗНЗЈеЙЪОГіСЫбљЦЗМфЕФЯрЫЦадКЭВЛЯрЫЦад,ФмШУЮвУЧдкНјаае§ЪНЕФМьбщжЎЧАЖдгкФмМьВтЕНЖрЩйВювьБэДяЛљвђгаИіДѓжТИХФюЁЃРэЯыЧщПіЯТ,бљБОЛсдкИїИіЪЕбщзщФкКмКУЕФОлРр,ЧвЮвУЧПЩвдМјБ№ГідЖРыЫљЪєзщЕФбљБО,ВЂзЗзйЮѓВюЛђЖюЭтЗНВюЕФРДдДЁЃШчЙћДцдкЕФЛА,ММЪѕжиИДгІЕБЛЅЯрЗЧГЃНгНќЁЃ
етбљЕФЭМПЩвдгУlimmaжаЕФplotMDSКЏЪ§ЛцжЦЁЃЕквЛИіЮЌЖШБэЪОФмЙЛзюКУЕиЗжРыбљЦЗЧвНтЪЭзюДѓБШР§ЕФЗНВюЕФСьЯШБЖЪ§БфЛЏ(leading-fold-change),ЖјКѓајЕФЮЌЖШЕФгАЯьИќаЁ,ВЂгыжЎЧАЕФЮЌЖШе§НЛЁЃЕБЪЕбщЩшМЦЩцМАЕНЖрИівђзгЪБ,НЈвщдкЖрИіЮЌЖШЩЯМьВщУПИівђзгЁЃШчЙћдкЦфжавЛаЉЮЌЖШЩЯбљБОПЩАДееФГвђзгОлРр,етЫЕУїИУвђзгЖдгкБэДяВювьгагАЯь,дкЯпадФЃаЭжагІЕБНЋЦфАќРЈНјШЅЁЃЗДжЎ,УЛгаЛђепНігаЮЂаЁгАЯьЕФвђзгдкЯТгЮЗжЮіЪБгІЕББЛЬоГ§ЁЃ
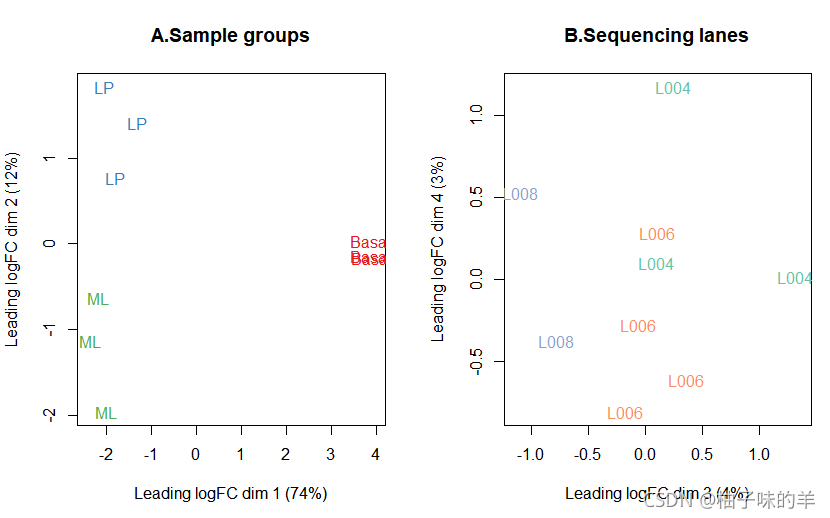
дкетИіЪ§ОнМЏжа,ПЩвдПДГібљБОдкЮЌЖШ1КЭ2ФмКмКУЕиАДееЪЕбщЗжзщОлРр,ЫцКѓдкЮЌЖШ3АДееВтађгОЕР(бљЦЗХњДЮ)ЗжРы(ШчЯТЭМЫљЪО)ЁЃгЩгкЕквЛЮЌЖШНтЪЭСЫЪ§ОнжазюДѓБШР§ЕФЗНВю,ЮвУЧЛсЗЂЯжЕБЙизЂИќИпЮЌЖШЪБ,ЮЌЖШЩЯЕФШЁжЕЗЖЮЇЛсБфаЁЁЃ
ОЁЙмЫљгабљБОЖМАДзщОлРр,дкЮЌЖШ1ЩЯзюДѓЕФзЊТМВювьГіЯждкbasalКЭLPвдМАbasalКЭMLжЎМфЁЃвђДЫ,дЄЦкдкbasalбљЦЗгыЦфЫћжЎМфЕФГЩЖдБШНЯжаФмЙЛЕУЕНДѓСПЕФDEЛљвђ,ЖјдкMLКЭLPжЎМфЕФБШНЯжаЕУЕНЕФDEЛљвђЪ§СПТдЩйЁЃдкЦфЫћЕФЪ§ОнМЏжа,ВЛАДееЪЕбщзщОлРрЕФбљБОПЩФмдкЯТгЮЗжЮіжажЛБэЯжГіНЯаЁЕФЛђВЛБэЯжГіВювьБэДяЁЃ
ЮЊЛцжЦMDSЭМ,ЮвУЧЮЊВЛЭЌЕФвђзгЩшСЂВЛЭЌЕФХфЩЋЁЃЮЌЖШ1КЭ2вдЯИАћРраЭЩЯЩЋ,ЖјЮЌЖШ3КЭ4вдВтађгОЕР(ХњДЮ)ЩЯЩЋЁЃ
#ЛцжЦMDSЭМ
lcpm<-cpm(x,log=TRUE)
par(mfrow=c(1,2))
col.group<-group
levels(col.group)<-brewer.pal(nlevels(col.group),"Set1")
col.group<-as.character(col.group)
col.lane<-lane
levels(col.lane)<-brewer.pal(nlevels(col.lane),"Set2")
col.lane<-as.character(col.lane)
plotMDS(lcpm,labels = group,col=col.group)
title(main = "A.Sample groups")
plotMDS(lcpm,labels = lane,col=col.lane,dim=c(3,4))
title(main = "B.Sequencing lanes")
дЫааНсЙћ
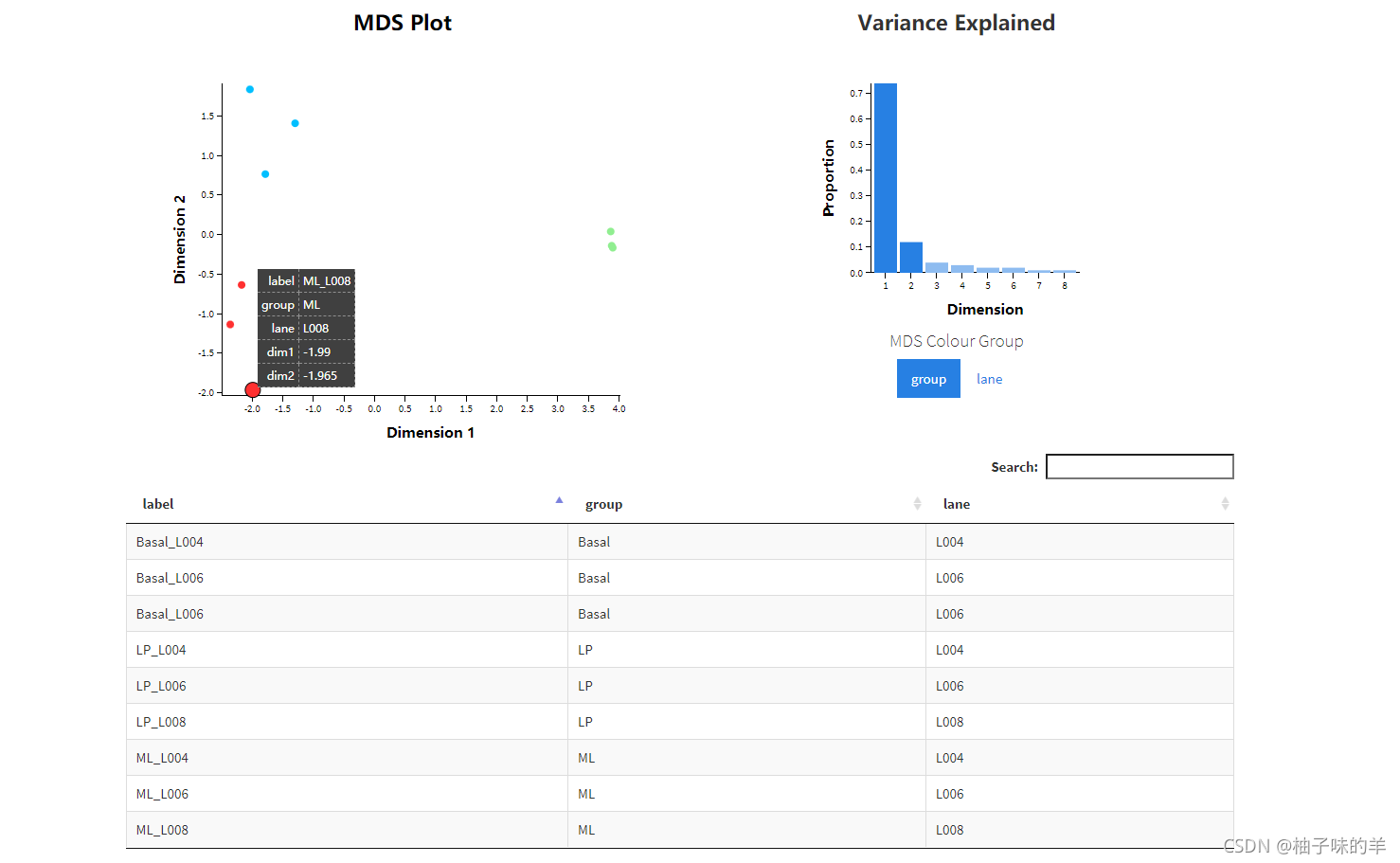
ЪЙгУGlimmaжаЕФglMDSplotКЏЪ§ПЩвдЕУЕННЛЛЅЪНMDSЭМЁЃЦфжаЕФglMDSPlotКЏЪ§ПЩЩњГЩвЛИіhtmlЭјвГ(ШчЙћЩшжУlaunch=TRUEВЮЪ§,НЋЛсдкЩњГЩКѓжБНгдкфЏРРЦїжаДђПЊ),ЦфзѓВрУцАхКЌгавЛеХMDSЭМ,ЖјгвВрУцАхАќКЌвЛеХеЙЪОСЫИїИіЮЌЖШЫљНтЪЭЕФЗНВюБШР§ЕФжљаЮЭМЁЃЕуЛїжљаЮЭМжаЕФжљПЩЧаЛЛMDSЭМЛцжЦЪБЫљЪЙгУЕФЮЌЖШ,ЧвНЋЪѓБъаќИЁгкЕЅИіЕуЩЯПЩЯдЪОЯргІЕФбљБОБъЧЉЁЃвВПЩЧаЛЛХфЩЋЗНАИ,вдЭЛЯдВЛЭЌЯИАћРраЭЛђВтађгОЕР(ХњДЮ)ЁЃ
glMDSPlot(lcpm, labels=paste(group, lane, sep="_"),
groups=x$samples[,c(2,5)], launch=TRUE)
дЫааНсЙћ
аЁНс:НёШеИцвЛЖЮТф,УїШеМЬај~